TECHNISCHES PAPIER #25
UNDERSTANDING BATTERIEN
Durch
Lee Merriman
Technische Rezensenten
J.F.
Douglas
James H. Hahn
Lester H. Smith, Jr.
Published Durch
VITA
1600 Wilson Boulevard, Zimmerflucht 500,
Arlington, Virginia 22209 USA
TEL:
703/276-1800. Fax: 703/243-1865
INTERNET:
pr-info@vita.org
Understanding Batterien
ISBN:
0-86619-225-5
[C]1985, Freiwillige in Technischer Hilfe,
PREFACE
Dieses Papier ist eine einer Folge, die von Freiwilligen in Technisch veröffentlicht wird,
Hilfe, eine Einführung für bestimmte Staat-von-der-Kunst bereitzustellen
Technologien von Interesse zu Leuten in Entwicklungsländern.
Die Dokumente werden beabsichtigt, als Richtlinien benutzt zu werden, um zu helfen
Leute wählen Technologien, die zu ihren Situationen geeignet sind.
Sie werden nicht beabsichtigt, Konstruktion oder Implementierung bereitzustellen
details. People werden gedrängt, VITA oder eine ähnliche Organisation zu verständigen
für weitere Informationen und technische Hilfe wenn sie
Fund, den eine besondere Technologie scheint, ihren Bedürfnissen zu entsprechen.
Die Dokumente in der Folge wurden geschrieben, wurden überprüft, und wurden illustriert
fast ganz von VITA Volunteer technische Experten auf ein rein
freiwilliger basis. , den Einige 500 Freiwillige in die Produktion verwickelt wurden,
von den ersten 100 Titeln, die ausgestellt werden, und trägt ungefähr bei
5,000 Stunden von ihrem time. VITA, die Personal Maria Giannuzzi einschloß,
als Redakteur, Suzanne Bäche-Behandlung-typesetting und Anordnung, und
Margaret Crouch als Projekt-Manager.
Der Autor dieses Papieres, VITA Freiwilliger Horace McCracken, ist das
Präsident der McCracken Solaren Gesellschaft in Alturas, Kalifornien.
Der Mitverfasser, VITA Freiwilliger Joel Gordes, ist gegenwärtig das solar
planen Sie Analytiker für den Staat von Connecticuts Solar Mortgage
Subvention Program. The, den Rezensenten auch VITA volunteers. Daniel sind,
Dunham hat das Konsultieren in solaren und alternativen Quellen von gemacht
Energie für VITA und AID. He hat gelebt und hat in Indien, Pakistan, gearbeitet
und Morocco. Mr. Dunham hat auch eine Staat-von-der-Kunst vorbereitet
untersuchen Sie auf solaren Destillierapparaten für HILFE.
Jacques Le Normand ist Assistent
Direktor beim Stütze-Forschung-Institut, Quebec, Kanada,
welcher forscht in erneuerbarer Energie.
, den Er Arbeit beaufsichtigt hat,
mit solaren Sammlern und hat mehreren publiations auf geschrieben
solar und Wind-Energie, und Erhaltung.
Darrell G. Phippen ist ein
mechanischer Ingenieur und Entwicklung-Spezialist, mit denen zusammenarbeiten,
Essen für das Hungrig in Scottsdale, Arizona.
VITA ist ein Gefreiter, gemeinnützige Organisation, die Leute unterstützt,
das Arbeiten an technischen Problemen in Entwicklungsländern.
VITA Angebote
Informationen und Hilfe richteten bei behilflichen Individuen und
Gruppen auszuwählen und Gerät-Technologien eignen zu an ihr
situations. VITA behält einen internationalen Anfrage-Dienst bei, ein
spezialisiertes Dokumentation-Zentrum, und ein computerisierter Dienstplan von
Freiwilliger technische Berater; leitet langfristige Feld-Projekte;
und veröffentlicht eine Vielfalt von technischen Handbüchern und Dokumenten.
UNDERSTANDING BATTERIEN
Von VITA Freiwilliger Lee Merriman
I. INTRODUCTION
Batterien sind im Gebrauch viele Jahre gewesen, aber heute gibt es ein
größere Forderung für Batterie-Macht als je vor.
, den Dies erneuerte,
Interesse ist nicht nur von neuen Entwicklungen herbeigeführt worden, aber
auch durch die Vielfalt von Verwendungen für Batterien in Zivilisten, industriell,
und militärische Anwendungen.
Dieses Papier stellt ein Grund Verständnis von Batterien und Spuren bereit
ihre Entwicklung von den frühen 1800s zum gegenwärtigen day. Research
und Entwicklung setzt in einer Anstrengung zu lösen fort das eigen
Schwäche von Batterien nämlich, wie mehr Energie zu packen ist,
in ein kleineres Paket.
Eine elektrische Zelle oder Batterie ist ein Gerät, das umgestaltet, das
chemische Energie enthielt direkt innerhalb seiner aktiven Materialien
in elektrische Energie mittels einer electrochemical-Reaktion.
Diese Art von Reaktion bringt die Übertragung von Elektronen von einem mit sich
noch ein durch eine führende Lösung materiell.
Historically,
Batterien spielten in den frühen Tagen eine wichtige Rolle von elektrisch
Entwicklung beide in den Vereinigten Staaten und in Europa.
In 1800 nannte ein italienischer Wissenschaftler, daß Volta entdeckte, daß durch
zwei unterschiedliche Schaffner in einer chemischen Lösung eintauchend ein
electromotive zwingen (EMF) oder Spannung wurde dazwischen geschafft das
zwei conductors. Figure 1 illustriert eine einfache Voltaic Zelle.
ub1x1.gif (393x393)

Die festen Schaffner der Zelle werden Elektroden gerufen und das
das Führen von Flüssigkeit der Elektrolyt.
, den EINE Zelle aus zwei Elektroden besteht,
und ein electrolyte. EINE Batterie besteht aus einem oder mehr
cells. Die Spannung der Zelle hängt auf dem Material von ab das
Elektroden und der Elektrolyt.
Die elektrische aktuelle Ausgabe und
die Macht der Zelle ist auf den Teller-Dimensionen abhängig und
das Gewicht des Elektrode-Materials.
Es gibt im Gebrauch zwei allgemeine Arten von Batterien heute: die Urwahl
tippen Sie oder " trockene Zelle " und die sekundäre Lagerung battery. EIN
primäre Batterie produziert eine Strömung durch Begleichung-Handlung wenn ein
von den Elektroden der Zelle wird während Verwendung zerlegt.
Diese Art
von Zelle kann wieder durch das Nachladen zu benutzen nicht wiederhergestellt werden und das
ganze Zelle muß weggeworfen werden, wenn es nicht mehr active. Secondary ist,
Zellen sind andererseits chemisch umkehrbar und Dose
würde beauftragt und würde über vielen Zyklen von Bedienung vorher geloschen
werdend ersetzt.
In der einfachen Spannung-Zelle, die in Zahl 2 gezeigt wird, wenn zwei unterschiedlich
ub2x3.gif (486x486)
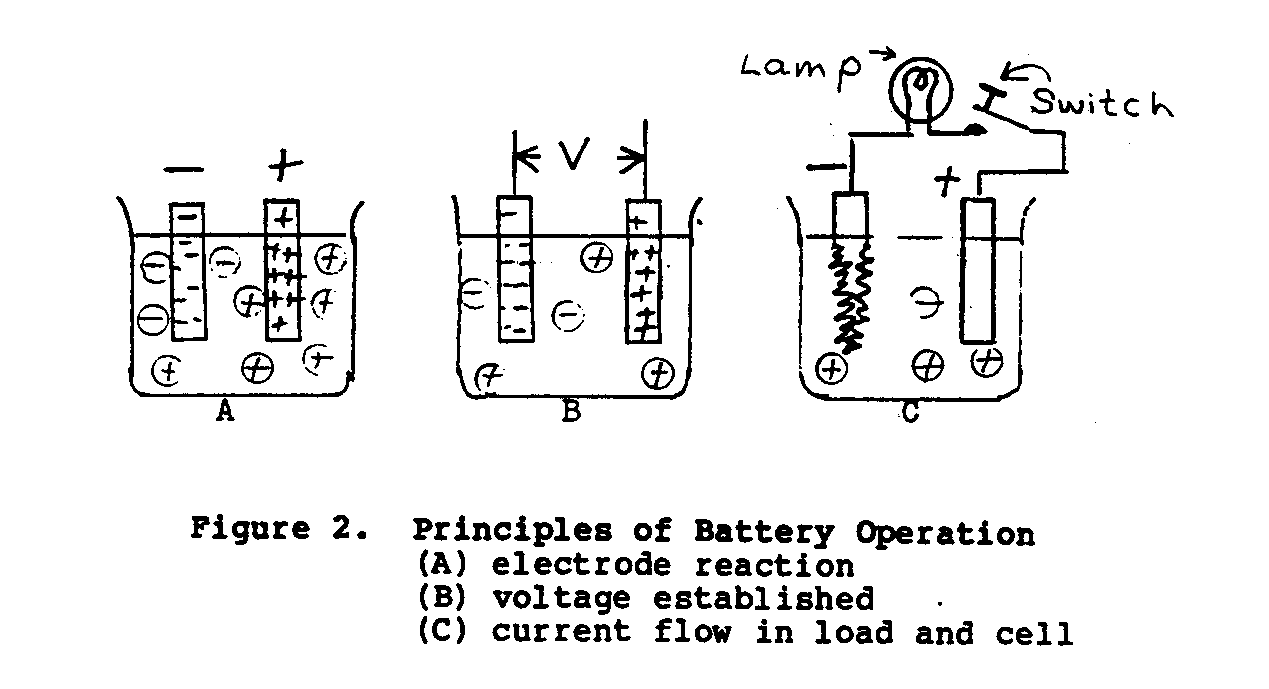
Metalle, Zink und Kupfer, werden in einem Elektrolyten von aufgehängt
verdünnen Sie sulfuric-Säure, ein Potential von approxiamtely 1.10 Volt
werden Sie zwischen den Elektroden existieren.
, den Die Zink-Elektrode sein wird,
negativ und die kupferne Elektrode wird bestimmt sein.
Wenn das
wechseln Sie in der externen Last-Schaltung, wird geschlossen, ein aktueller Wille
fließen Sie durch die Last (das Energie-aufnehmen von Gerät) und Batterie in
Übereinstimmung zum Gesetz von Ohm. (*) Als die Last-Strömung setzt fort, zu fließen,
Wasserstoff als Blasen wird erscheinen und wird den kupfernen Teller decken, und
der Zink-Teller wird allmählich auflösen.
Der Haupt Nachteil
mit dieser Zelle ist, daß das Gas sprudelt, nehmen Sie zu das innerer
Widerstand der Zelle, beim Verursachen von aktueller Ausgabe, abzunehmen.
-------- -------- ------
(*) Der Gleichstrom, der in einer elektrischen Schaltung fließt, ist direkt
der Spannung, die zur Schaltung angewandt wird, verhältnismäßig.
Die Konstante
von Proportionalität R, rief den elektrischen Widerstand, wird gegeben
durch die Gleichung V = RI, in dem " V " die angewandte Spannung ist, und
Ich " bin die Strömung.
IIE. TECHNOLOGIE-VARIATIONEN
PRIMÄRE BATTERIEN
Mehrere andere Arten von primär-Typ, die nasse Zellen entwickelt wurden,
und gebraucht in den Vereinigten Staaten.
Most bemerkenswert unter diesen war das
Schwerkraft-Zelle, die ätzend-Kupfer-Oxid-Zelle, die Luft-erschütterten,
Zelle, und die Lelanche Zelle.
, den Jede Zelle sein eigenes Operieren hatte,
Merkmale, und aktuelle Kapazitäten schwankten von weniger als einem
Ampere (Ampère) für die Lelanche Zelle zu mehreren hundert Ampere für
die ätzend-Kupfer-Oxid-Zelle.
, den Die britische Post entwickelte,
eine nasse Zelle, die als die Zelle des Daniels gewußt wird, die mehrere anbot,
hervorragende operierende Merkmale.
Es gab zwei Haupt Schwierigkeiten mit der primär-Typ-Zelle
Konstruktion, Verschlechterung durch örtliche Handlung und Zelle-Polarisation.
Örtliche Handlung ist eine innerere chemische Handlung zu eigen
Batterien; das Leben der Zelle wird allmählich sogar verringert
obwohl keine Last zu seinen Terminals verbunden wird.
Local Handlung ist
definierte genau als die Begleichung von aktivem Material von ein von beiden Teller
zu irgendeiner Verunreinigung im Elektrolyten oder dem Teller-Material.
Dieses
Handlung verursacht die Formation von kurzgeschließten Zellen, die verursachen,
das Metall, sich zu verschlechtern.
Zell Polarisation wird von Wasserstoff-Blasen verursacht, die eingezahlt werden,
auf der Kathode wenn aktuelle Strömungen durch die Zelle.
, den Dies herunterläßt,
die Grenz Spannung und die Zunahmen der innerere Widerstand von das
battery. Various Methoden für das Neutralisieren dieser polarisierenden Wirkung
wurde benutzt, entweder neben chemischer oder mechanischer Konstruktion der
führte zur Entwicklung der Luft-erschütterten Zelle.
In der Luft-erschütterten Zelle wurde die Elektrode von gemacht ein sehr
Absorbens-Form von Kohlenstoff und wurde über dem Elektrolyten aufgehängt
level. , weil die Kohlenstoff-Elektrode nicht im Elektrolyten eingetaucht wurde,
Lösung, Polarisation der Zelle wurde verhindert.
In
Bedienung, Sauerstoff, der die poröse Oberfläche des Kohlenstoffes umgibt,
Elektrode kombiniert mit dem Wasserstoff, der bei der Oberfläche von entwickelt wird,
die Kohlenstoff-Elektrode und der Elektrolyt.
Good Belüftung wurde erfordert
um eine befriedigende Luft-Versorgung für Bedienung beizubehalten.
Das
Edison Kohlenstoff Zelle und die Carbonaire Batterie waren repräsentativ
von der Luft-erschütterten Art.
Wet primär-Typ-Zellen haben zum größten Teil
geworden von der sekundär-Typ-Lagerung-Batterie ersetzt.
Der moderne Tag " trockene Zelle, " die von George entwickelt wurde,
Lelanche in 1868, ist eine Modifikation vom alten Lelanche nasse Zelle.
Der Unterschied ist das, nur genügendes Wasser wird zu hinzugefügt das
Elektrolyt, ein Absorbens-Futter anzufeuchten.
Die moderne trockene Zelle
ist hauptsächlich der überall benutzte aller primären Batterien heute
wegen ihres niedrigen Preises, zuverlässige Aufführung, und weitverbreitet
availability. Dry, den Zell Batterien in Klassen von 1.5, 3, gemacht werden,
6, 7.5, 9, 22.5, 45, 67, und 90 Volt.
Die gewöhnlichste Art von Konstruktion für eine trockene Zelle wird in gezeigt
Glauben Sie 3.
ub3x4.gif (486x486)

Die Zelle in Zahl 3 Verwendungen ein Kohlenstoff-Stab für die Anode oder bestimmt
Terminal und ein Außen Zink-Container (Fall) für die Verneinung
terminal. , den Der Zink-Fall ein inneres Futter von Absorbens-Papier hat,
Material, das mit dem Elektrolyten gesättigt wird.
Der Raum
zwischen den Elektroden wird mit einer Mischung von zerdrückter Coca-Cola gefüllt,
Mangan-Dioxyd, und Graphit.
Manganese wird als ein depolarizer hinzugefügt.
Der Elektrolyt ist salammonic und Zink-Chlorid.
Das
Spitze des Falles wird mit einer siegelnden Verbindung und dem Zink gesiegelt
Container wird in einem papierähnlichen Container eingeschlossen.
Die Spannung von ein neu
trockene Zelle sind 1.4 bis 1.6 Volt.
Trockene Zell Batterien fallen in drei allgemeine Klassen: (1) Taschenlampe
Batterien normalerweise 1-1/4 Zoll in Durchmesser und 2-1/2 Zolln
hoch mit einer aktuellen Kapazität von ungefähr 3 Ampère-Stunden; (2) große Größe
Zellen, die im allgemeinen zu als die Zahl 6 trockene Zelle ungefähr gesprochen werden,
2-1/2 Zoll in Durchmesser und 6 Zoll hoch mit ein
aktuelle Klasse von ungefähr 30 Ampère-Stunden; und (3) die " schwere Pflicht "
und hohe Spannung, die eine Zelle oder eine Kombination sein könnte, tippt
von Zellen, gebraucht in industriellem Dienst mit aktuellen Kapazitäten von
50 Ampère-Stunden oder greater. , von denen Die Ampere-Stunde-Kapazität die Rate ist,
löschen Sie, eine Batterie kann eine gegebene Periode von Zeit beibehalten,
normalerweise acht hours. zum Beispiel schätzte eine 30 Ampère-Stunde Batterie ein
normal konnten acht Stunden ungefähr 3-1/2 Ampère liefern.
Als gewöhnlich
aber benutzt, stellen trockene Zellen weniger als ihre Klasse bereit.
Das Regal-Leben wird von örtlicher Handlung begrenzt und aus dem Grund
einige Hersteller stempeln ein Dienst-Datum auf dem äußeren Belag von
jeder cell. Local Handlung verursacht schließlich Verschlechterung von das
Batterie, und nach ungefähr einen oder zwei Jahre-Lagerung, die Batterie
wird useless. , weil die Zink-Elektrode Teil von bildet, das äußer
umgeben Sie mit einer Mauer, seine allmähliche Zerstörung schwächt die Zell Struktur, und als
das entwickelte Wasserstoff-Gas baut innereren Druck auf, es kann
brechen Sie und verschütten Sie seine zerstörende Inhalte.
aus diesem Grund, Ausrüstung
sollte nie mit trockenen Zellen im Verlauf langer Perioden von gelagert werden
time. Dry Zellen erfordern keine Aufrechterhaltung und wenn sie nicht mehr
operieren Sie, wird weggeworfen und wird ersetzt.
Eine letzt Art trockener Zelle, die entwickelt wird, ist der Ruben oder Merkur
Zelle (Zahl 4) . This, durch den Zelle während zweite Weltkrieg entwickelt wurde,
ub4x6.gif (600x600)
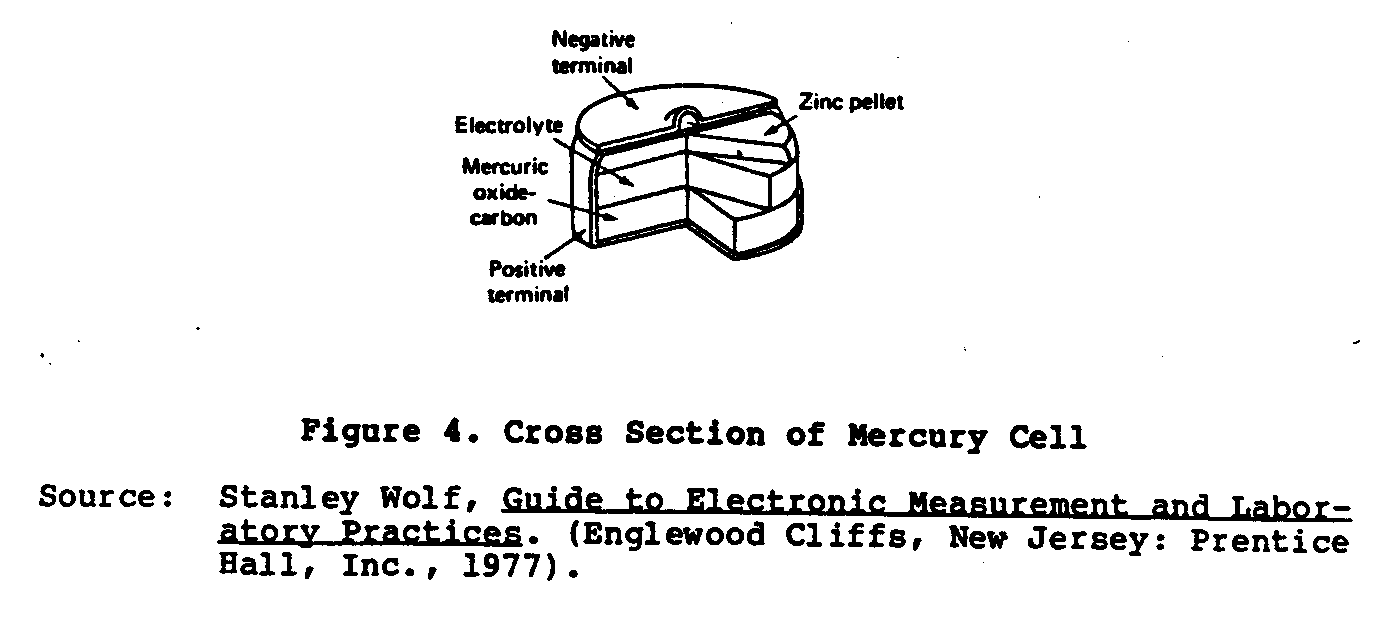
Ruben Laboratories und P.R. Mallory Gesellschaft für das klein Operieren
elektronische Ausrüstung, die hohe aktuelle Macht erfordert.
, den Diese Zelle ist,
machte in zwei Formen: die " Rolle-Anode " und der " Knopf tippen. " The
Anode wird Zink fusioniert, und die Kathode ist ein Quecksilber Oxid
erschüttertes Material mischte mit Graphit.
Der Elektrolyt ist ein
Lösung von Kalium-hydroxide (KOH) das Enthalten von Kalium-zincate.
Diese Zellen sind weit trockenes Zelle Schulden zum Lelanche überlegen
zu ihrer kompakten Größe, flache Spannung-Eigenschaft, und sehr lang
Regal life. , den Die Leerlaufe Spannung dieser Zellen 1.34 Volt sind.
Mehrere anspruchsvolle Entwicklungen sind in kleinen Batterien gemacht worden,
beide primär und sekundär-Typ-Zellen, die einschließen, das
Magnesium, alkalisch, Silber-Zink, und lithium.
Tisch 1 Listen das
ubxtab1.gif (600x600)

Merkmale und Anwendungen dieser Zellen.
SEKUNDÄRE LAGERUNG-BATTERIEN
Seit 1965, dort ist Interesse im Benutzen von Lagerung erneuert worden
Batterien in Macht systems. , den Dies ist, weil moderner Macht-Verbrauch
bringt sehr unebene Last-Forderungen mit sich und das Vergrößern von Höhepunkt-Last
demands. , Wenn ein System mehr Macht liefern muß, (Zunahme in Last
Forderung), der Lieferant kann die Forderung erfüllen, indem er entweder wechselt, ein
zusätzlicher Generator auf das System oder das Wechseln ein beauftragte
Batterie-Bank auf den line. Das letzt erfordert ein viel kleiner
Anlage.
Die Wiederbelebung von Batterien als Macht-System-Einheiten hat hauptsächlich
angefangen mit kleinen unabhängigen Systemen wie Wind-oder Wasser-angetrieben
generators. In solchen Systemen, Lagerung-Batterien treten auf
zwei wichtige functions. First, während Perioden niedriger Last-Forderung,
die System-Batterie kann viel der erzeugten Energie lagern,
welcher würde ansonsten zum System verloren werden.
Second, Energie,
während der verkehrsschwachen Periode gelagert, ist während Zeiten von verfügbar
Höhepunkt-Last demand. Die Wichtigkeit von das letzt kann illustriert werden
mit dem folgenden quantitativen Beispiel: Nehmen Sie ans
Kapazität der Batterie hat einen Begleichung Macht Rate Gleichgestellten zu Seite
von der Generator-Macht-Kapazität ([P.sub.B] = 0.5 [P.sub.G]) . This bedeutet das
unter normalen Zuständen, während Perioden hoher Last-Forderung, das
Generator-Batterie-Kombination kann mehrere Stunden, dienen Sie einer Last
von bis zu 1.5 Malen das was der Generator allein konnte dienen.
Noch ein Grund für das zugenommene Interesse an sekundärer Lagerung
Batterien sind das Bedürfnis für Unterstützung-Macht für einige von das neuer
technology. zum Beispiel bringen modernste Computer irgendeine Form mit sich
von " flüchtiger " Lagerung von Informationen ist das, die Informationen sind
verlor, wenn Macht removed. ist, gegen diese Möglichkeit zu beschützen, viel,
Computer-Systeme benutzen " uninterruptible "-Macht-Systeme, die auf gegründet werden,
Lagerung-Batterien, um elektrische Strömung zum Computer zu liefern,
Ausrüstung, wenn kommerzielle Macht verloren wird.
Die Lagerung-Batterie, die mit sekundären nassen Zellen konstruiert wird, ist
ähnlich in Handlung zu einer primären Zelle, außer den chemischen Handlungen,
betroffen, ist praktisch vollkommen umkehrbar.
, Sobald die Zelle ist,
losch, Strömung von einer externen Quelle, ging durch vorbei das
Zelle in der gegenüberliegenden Richtung, wird im wesentlichen wiederherstellen das
Batterie zu seinem Original beauftragte Zustand.
Es gibt gegenwärtig drei Arten von Lagerung-Batterien verfügbar:
(1) die Blei-Säure-Art; (2) das Nickel-Eisen oder alkalische Batterie
(Edison Zelle); und (3) das Nickel-Kadmium oder der Alkali-Typ (Nicad).
Blei-Säure-Batterien
Die Blei-Säure-Batterie ist die am überall gebrauchte Art von Batterie
heute wegen seines niedrigen Preises, Zuverlässigkeit, gute Aufführung,
Merkmale, und breite Anwendung.
, den Diese Batterie hergestellt wird,
in vielen Größen und Kapazitäten, die von 1 Ampère-Stunde bis zu schwanken,
mehrere tausend Ampère-Stunden-Klasse. (*)
Die Lagerung Zell benutzt reaktives Schwamm-Blei für die Verneinung
Elektrode (Pb), Blei-Dioxyd für die bestimmte Elektrode (Pb0),
und verdünnt sulfuric-Säure für den Elektrolyten.
Die Elektrode
Materialien haben kleine strukturelle Stärke und müssen unterstützt werden
auf Tellern oder grids. hat Das Gitter des Batterie-Tellers zwei Funktionen:
zuerst unterstützt es das aktive Teller-Material; und Sekunde,
es dient als ein Schaffner, um das Teller-Terminal zu allen zu verbinden
Teile des aktiven Materials.
Führen Sie, Lagerung-Batterie-Teller werden in zwei Arten geteilt, das
Plante (bildete) und der Faure (kleisterte), wie in Zahl 5. In gezeigt
ub5x9.gif (600x600)

der Plante-Typ von Konstruktion, den das aktive Material elektrisch ist,
bildete von reinem Blei durch einen electrochemical-Prozeß von das
metallisches Blei des unterstützenden Gitters.
Im Faure-Typ das
aktives Material wird auf dem unterstützenden Gitter in der Form von angewandt
ein Paste-follwed neben einem Rahmen, beim Trocknen, und das Bilden von Bedienung.
Glauben Sie 5 Shows der Plante (EIN) und Faure (B) Blei Zell plates. Das
Zell Versammlungen werden zusammen gelötet, um bestimmt und negativ zu bilden
Gruppen, die zusammen verzahnt werden, um wieder zu vertragen, das vollständig
Batterie, die cell. Separators zwischen die Elektroden gesetzt werden,
und das vollständige Element wird in einen Container und sealed. gesetzt Das
Verwendung großer Teller mit nahem Abstand begrenzt den innereren Widerstand
von der Batterie zu einem niedrigen Niveau.
Figure 6 Shows ein Schnitt
ub6x9.gif (600x600)

Sicht der Blei-Lagerung-Zelle.
Während Begleichung die Batterie materiell von beiden Tellern wird konvertiert
in Blei sulfate. , den Die Menge von Blei-sulfate onthe-Teller bildete,
und die Menge von Säure verlor vom Elektrolyten, ist in genau
Verhältnis zur Rate von Begleichung.
Die umgekehrten Handlung-Aufnahmen
Stelle, wenn die Zelle beauftragt wird.
Zelle, die chemische Reaktionen sind,
stellte durch die folgende Gleichung dar; aber dies ist ein
vereinfachte Form, als die eigentliche Handlung sehr mehr kompliziert wird.
-------- -------- -------
(*) Batterie-Ampere-Stunde-Klasse wird normal auf einer 8-Stunde-Begleichung gegründet
Rate.
Beim bestimmten Teller:
PB[O.SUB.2] + HS[O.SUB.4][SUP .-] + [3H.SUP.+] + [2E.SUP .-] (* )-----> PB[SO.SUB.4] + 2[H.SUB.2]O
Beim negativen Teller:
Pb + HS[O.sub.4][sup .-]---- -> Pb[SO.sub.4] + [H.sup.+] + [2e.sup .-]
Sowohl die kombinierte Zell Reaktion für Begleichung als auch Gebühr wird ausgedrückt
durch die folgende Gleichung:
löschen
------ ------->
Pb[O.sub.2] + Pb + 2[H.sub.2] S[O.sub.4] <= == == = 2Pb[SO.sub.4] + 2[H.sub.2]O + elektrische Energie
SULFURIC
plate -plate ätzende Teller
<------ -------
beauftragen
Auf Begleichung die ätzenden Einzelteile vom Elektrolyten und den Formen ein
chemische Kombination mit den Tellern, das Verändern davon, um sulfate zu führen.
Als Begleichung fortsetzt, wird zusätzliche Säure von gezeichnet das
Elektrolyt bis Strömung wird aufhören, zu fließen.
Das Wasser, bildete
durch den Verlust von Säure zu den Tellern, läßt herunter das bleibend bestimmt
Schwerkraft (* *) vom Elektrolyten.
In allgemeine Praxis, Begleichung ist
immer hielt, bevor die Teller sulfated ganz haben, weil
einmal ganz sulfated, Batterie-Zustand kann nicht konvertiert werden
aktivem Material auf Gebühr hinter.
Auf Gebühr die umgekehrte Handlung
Aufnahmen setzen: die Säure in den sulfated-Tellern wird in hinter gefahren
der Elektrolyt, und der S[O.sub.4] kombiniert mit Wasserstoff im Wasser
um zusätzliche sulfuric-Säure zu bilden ([H.sub.2][SO.sub.4]).
Elektrolyt für Blei-Säure-Zellen sollte sulfuric acid. Für verdünnen ein
vollständig beauftragte Batterie, zu der die bestimmte Schwerkraft von 1.200 variiert,
1.30 und wenn 1.150 geloschen hat (reines Wasser mißt 1.00) . The
bestimmte Schwerkraft wird von einem Spritze-Typ-Hydrometer als gemessen
gezeigt in Zahl 7, und Werte sind Temperatur, die korrigiert wird.
ub7x11.gif (600x600)

-------- -------- --------
(*) Das Symbol e-steht für Elektronen.
(* *) Bestimmte Schwerkraft wird als das Verhältnis von Gewicht von definiert ein gegeben
Volumen einer Substanz zu einem gleichen Volumen reinen Wassers.
Die Spannung einer Blei-Zelle sind ungefähr 2.10 Volt bei keiner Last
aber ist höher, als werdend beauftragt.
Normal Spannung auf Gebühr ist
2.15 Volt und als das Zell nähert volle Gebühr dieser Wert
schnell Zunahmen zu zwischen 2.5 und 2.6 Volt.
Dieses spätere Intervall
von Gebühr wird als die " begasende Periode " gewußt.
Von begasend das
Elektrolyt zu irgendeiner Zeit während des Beauftragen sollte als vermieden werden das
Gebühr-Rate ist auch high. Als eine Zelle, erreicht sein letzt vollständig
Zustand beauftragt, ist eine hohe Strömung als dieser Überschuß nicht ratsam
Strömung zerlegt das Wasser im Elektrolyten, der gefahren wird,
von in der Form von Gas.
Die Blei-Säure-Batterie hat mehrere Nachteile:
(1) Zellen sind
Temperatur empfindsam und verliert Macht in kalten Temperaturen; (2)
Zell Teller tendieren, zuzuschnallen und auf ausdauernder, hoher Strömung zu verfälschen
Dienst, und (3) besondere Sorge muß beobachtet werden, wenn eine Batterie ist,
lange Perioden nicht benutzt, ansonsten wollen die Zellen sulfate.
Nickel-Eisen-Batterien
Das Nickel-Eisen oder alkalische Batterie wurde entwickelt, um zu überwältigen das
eigene Nachteile der Blei-Teller-Zelle.
, den Es ein Radikaler ist,
Abreise von ihm in sowohl Konstruktion als auch Bedienung.
Ins
Vereinigte Staaten, die diese Batterie als die " Edison Zelle gewußt wird, nannte "
nach seinem Erfinder Thomas A. Edison.
Figure 8 Shows die Konstruktion
ub8x13.gif (600x600)
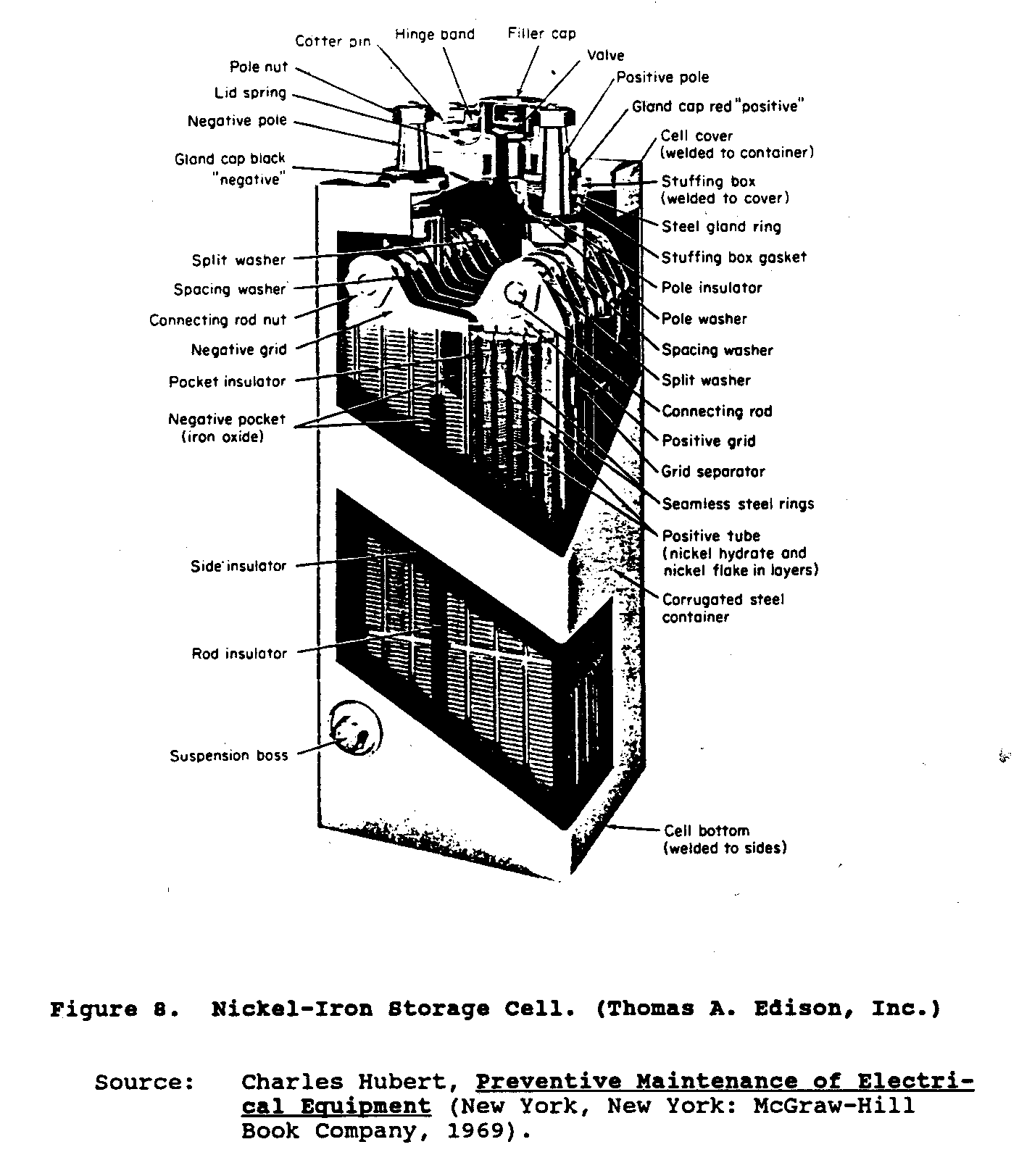
von einem typischen cell. besteht Der bestimmte Teller aus Stahl
Rohre, die Nickel-Hydrat und Nickel enthielten, fügten in Ersatz hinzu
layers. Der negative Teller wird von flachen Stahl-Kisten gebildet oder
Taschen, die perforiert werden und mit eisernen Oxid-Körnchen gepackt werden.
Laken-Stahl-Gitter unterstützen diese Rohre und die Taschen, die sind,
verriegelte zusammen, um bestimmte und negative Zell groups. Zelle zu bilden
Terminals und der Stahl-Container sind Nickel, das gepanzert wird.
Alle Separatoren
und das Isolieren von Teilen wird von Gummi gemacht.
Die Zelle benutzt ein
Elektrolyt von 21 prozentiger Lösung von ätzender Pottasche, die enthält, ein
kleine Menge von lithium-Hydrat.
Die Chemie dieser Zelle wird ziemlich kompliziert, und die Chemikalie
Reaktion, die in der Zelle vorkommt, ist als völlig anders
das des Bleies cell. , als der Der Elektrolyt bloß ein Führen fungiert,
mittler und betritt in Kombination mit keinen von das
aktives Teller-Material während Bedienung.
Seine bestimmte Schwerkraft
Überreste praktisch dauernd über dem vollständigen Zyklus von Gebühr
und discharge. Condition von Batterie-Gebühr oder Begleichung wird bestimmt
durch eine Spannungsmesser-Lektüre und nicht durch die bestimmte Schwerkraft von
der electrolyte. Die alkalische Batterie, die Zell Reaktion ist,:
löschen
------ -------- ---->
[Fe.sub.2] + 2NiOOH + KOH + 2[H.sub.2]O------ -> [Fe.sub.2][(OH) .sub.2] + 2Ni[(OH) .sub.2] + KOH + elektrisch
<------
<------ -------- --- Energie
CHARGE
Die Spannung jeder Zelle sind ungefähr 1.50 Volt auf, öffnen Sie
Schaltung, aber ist auf Gebühr höher und läßt unter Last-Zuständen herunter.
Diesen Batterien wird eine Ampere-Stunde-Kapazität-Klasse, die gegründet wird, gegeben
auf ihrer Rate von Begleichung bis zur letzten Spannung von 1.00 pro
cell. , den Einige aktuelle Klassen auf einer 5-1/2-Stunde ununterbrochen gegründet werden,
Begleichung-Rate, während andere auf einer 3-1/2-Stunde-Rate gegründet werden.
Anders als die Blei-Zelle-Batterie gibt es keine Minimum-Spannung hinunter
welcher diese Art von Zelle kann nicht geloschen werden.
in der Tat, diese Zelle
kann geloschen werden, um auf Null Volt zu setzen, der bei seinen Terminals kurzgeschließt wird,
und ging in diesen Zustand für eine unklare Periode.
Dieses
ist die Methode, durch die eine alkalische Batterie in Lagerung gesetzt wird.
Auch kann diese Zelle zuviel unbeabsichtigt berechnet werden, beauftragte ins
falsche Richtung, und schließte für einen Augenblick ohne Verletzung kurz.
Alkalische Batterien werden nicht verletzt, indem man friert, und ein Elektrolyt
mit einer bestimmten Schwerkraft von 1.200 um 15.5[degrees]C (60[degrees]F) friert fest
um-66[degrees]C (-87[degrees]F).
, den sich Der Elektrolyt dieser Zelle allmählich verschlechtert,
während Verwendung und muß schließlich verwandelt werden.
Die Haupt Vorteile der Nickel-Eisen-Zelle sind: (1) es ist
sehr Licht und starkes Schulden zu seiner Stahl-Konstruktion; (2)
es bietet ein unbegrenzt langes Leben an; und (3) es überwältigt das
Zell sulfating-Problem der Blei-Säure-Batterie.
Das Oberhaupt
Nachteil ist sein hoch zuerst kosten Sie und hoher innererer Widerstand.
Nickel-Kadmium-Batterien
Nickel-Kadmium oder Nicad Batterien, ein relativ neuer Zusatz zu
Lagerung-Zellen, wurde in Europa entwickelt.
, den Diese Batterien bestehen,
von verzahnten Versammlungen bestimmter und negativer Teller, die bestiegen werden,
in einem luftdicht verschlossene Stahl-Container.
Das bestimmte aktive Material, Nickel,
hydroxide, und das negative aktive Material, Kadmium-Oxid, ist
umhüllte in gleichen, fein perforierten Stahl-Taschen.
Die Teller
wird von Reihen von diesen Taschen, die gefältelt werden, wieder vertragen und
bildete in Stahl frames. Positive und negative Teller-Versammlungen
wird zusammen zu schweren Stahl-Bus-Stangen verriegelt.
Plate Gruppen sind
verzahnte und trennte durch dünne plastische Stäbe.
Die Zelle elektrisch
Terminals und Fall sind Nickel, das gepanzert wird.
Der Elektrolyt ist ein
Lösung besonders gereinigter ätzender Pottasche (Kalium-hydroxide)
löste in destilliertem Wasser auf.
Figure 9 Shows eine Schnitt Sicht
ub9x15.gif (600x600)

von der Nicad Batterie.
Die vereinfachte Zell Reaktion ist:
beauftragen
<------ -------- -----
Cd + 2NIOOH + KOH + 2[H.sub.2]O------> Cd[(OH) .sub.2] + 2Ni[(OH) .sub.2] + KOH + elektrisch
<------ Energie
------ -------- ------>
löschen
Während Gebühr oder Begleichung der Zelle gibt es praktisch nein
verändern Sie sich in der bestimmten Schwerkraft des Elektrolyten.
Like das
Edison Zelle, die einzige Funktion des Elektrolyten sollte als handeln ein
Schaffner für die Übertragung von Wasserstoff-Ionen von einer Elektrode zu
die other. , auf denen Die Spannung-Klasse jeder Zelle 1.20 Volt sind, öffnen
Schaltung; wenn zu einer externen Last verbunden hat, diese Spannung bleibt
ziemlich dauernd bis zu ungefähr 90 Prozent von sein bemessen
capacity. Die Ampère-Stunde-Klasse der Nicad Zellen hat auf basiert ein
letzte Begleichung-Spannung von 1.10 Volt pro Zelle.
Verschiedener Edison
Zellen, Nicad Batterien werden durch wiederholtes Über-löschen beschädigt werden
unter ihrem Minimum Zell Klasse von 1.10 Volt.
Nicad Batterien
haben Sie eine Temperatur, die Auswahl von-51[degrees]C operiert, (-60[degrees]F) zu 93[degrees]C
(200[degrees]F).
Nicad Batterien sind Vibration und Schock wegen immun ihr
Stahl-Konstruktion; Griff ihre Gebühr gut während lang müßig
Perioden; behalten Sie eine dauernde Spannung-Quelle während Begleichung bei; und
wird nicht durch beschädigt, berechnen Sie zuviel.
, in dem Diese Batterien bestiegen werden können,
keine stellen auf discharge. Like die Edison Zelle, die Nicad Batterie, auf
hat ein hoch zuerst kosten Sie wie mit der Blei-Säure-Batterie verglichen;
aber dieser hohe Preis wird von ihrem längeren Leben ausgeglichen
span. EIN Vergleich von Blei-Säure, alkalisch, und Nicad Batterien sind
präsentierte in Tisch 2.
Tisch 2.
Vergleich von Blei-Säure, Nickel-Eisen,
und Nickel-Kadmium-Batterien
Operating Zell Leben
Typical Temperatur Energie Gebühr /
Cell Auswahl Dichte Discharge Preis
TYPE VOLTAGE ([DEGREES]C) (WH (*) /KG) (CYCLES) ($/WH (*))
Blei-Acid 2.0 20 bis 30 37 1200-1500 .08
Nickel-Iron 1.2 2.2 bis 46 29
Nickel-Cadmium 1.25 (-51) zu 93 33
(* )Watt-Stunden
Allgemeine Aufrechterhaltung-Verfahren für Lagerung-Batterien
Richtige Aufrechterhaltung ist für fortgesetzten problemlosen Dienst wesentlich
von Lagerung batteries. , Während die Zell Konstruktion ander ist,
für die mehrere Arten ist Aufrechterhaltung für alle Arten ähnlich
und besteht aus den folgenden allgemeinen Verfahren:
1.
Keep Zellen reinigen und trocken;
2.
Check Elektrolyt-Niveau regelmäßig;
3.
Keep Batterien beauftragten jederzeit; und
4.
Keep Verunreinigungen aller Arten aus Zellen, als sie werden,
haben eine schädliche Wirkung und ruinieren schließlich them. Never
benutzen irgendwelche Werkzeuge oder Gebrauchsgegenstande (Hydrometer, Trichter, und so weiter)
, der zu Dienst andere Elektrolyten ander benutzt worden ist,
von dieses erforderlich für diese bestimmte Batterie,
besonders benutzten Werkzeuge für Blei-Säure-Batterien.
5.
Refer zu den Empfehlungen von Herstellern und bleibt ein
geschrieben Aufrechterhaltung-Aufzeichnung.
Der Elektrolyt der Blei-Säure-Zelle erfordert Ersatz nie
außer Verlust wegen unbeabsichtigter Stürze.
However, im Edison,
und Nicad Zellen es gibt eine allmähliche Verschlechterung ihres Elektrolyten,
welcher muß schließlich über dem Leben von ersetzt werden das
Batterie.
BIBLIOGRAPHY/SUGGESTED LEKTÜRE LISTE
Baumeister, T., Hrsg. Mark Übliche Handbuch für Mechanische Ingenieure.
7 Ausgabe. New York, New York,:
McGraw-Hügel-Buch
Gesellschaft, 1967.
CARR, C.C. Handwerks amerikanischer Elektriker Handbuch. 8 Ausgabe.
New York, New York,:
McGraw-Hügel-Buch-Gesellschaft, 1961.
Fink und Batey. Übliche Handbuch für Elektrische Ingenieure.
11
Edition. New York, New York,:
McGraw-Hügel-Buch-Gesellschaft, 1978.
Hubert, Charles I. Preventative Aufrechterhaltung Elektrischer Ausrüstung.
New York, New York,:
McGraw-Hügel-Buch-Gesellschaft, 1969.
Knowlton, A.E., Übliches Handbuch für Elektrische Ingenieure.
8
Edition. New York, New York,:
McGraw-Hügel-Buch-Gesellschaft, 1949.
McGraw-Hügel-Lexikon von Wissenschaft und Technologie. 5 Ausgabe.
New York, New York,:
McGraw-Hügel-Buch-Gesellschaft, 1982.
Timbre und Bush. Principles Elektrischen Ingenieurwesens.
3 Ausgabe.
New York, New York,:
Wiley und Söhne, AG, 1946.
Fressen Sie, Stanley. Guide zu Elektronischem Maß und Laboratorium
Practices.
Englewood Cliffs, New Jersey,: Prentice Korridor,
Inc., 1977.
== == == == == == == == == == == == == == == == == == == ==
== == == == == == == == == == == == == == == == == == == ==

